Números Quânticos: Guia Completo e Definições
Classificado em Física
Escrito em em  português com um tamanho de 4,65 KB
português com um tamanho de 4,65 KB
Números Quânticos
Os números quânticos descrevem as energias dos elétrons nos átomos e são de enorme relevância para determinar a posição e o comportamento dos elétrons nos átomos.

 Orbitais dos primeiros três níveis energéticos ("k", "l" e "m")
Orbitais dos primeiros três níveis energéticos ("k", "l" e "m")
Introdução
Existem quatro números quânticos principais:
- Número quântico principal;
- Número quântico de momento angular ou azimutal (secundário);
- Número quântico magnético;
- Número quântico de spin.
Estes quatro números quânticos permitem uma descrição completa dos elétrons nos átomos, definindo o nível principal de energia, o subnível, a orientação espacial da nuvem eletrônica e o spin do elétron. Cada combinação é única para um elétron.
Os três primeiros descrevem os orbitais atômicos, enquanto o quarto (spin) descreve o comportamento específico do elétron. Dois elétrons no mesmo orbital devem, obrigatoriamente, possuir spins opostos.
Número quântico principal (n)
O número quântico principal assume valores inteiros positivos. É o mais importante, pois define a energia do elétron e o tamanho do orbital.

Onde m e e são a massa e a carga do elétron, ε0 é a permissividade do vácuo e h é a constante de Planck. Esta equação deriva da mecânica quântica.
Número quântico de momento angular (l)
O número quântico de momento angular, ou azimutal, define a forma dos orbitais. Para um dado valor de n, l pode assumir valores inteiros de 0 a (n − 1).
Número quântico magnético (ml)
Especifica a orientação da nuvem eletrônica no espaço. Assume valores inteiros de -l a +l.
- l = 0: Subnível s (uma orientação).

 Subnível s: forma esférica.
Subnível s: forma esférica.
- l = 1: Subnível p (três orientações: px, py, pz).

 Subníveis p: orientados nos eixos cartesianos.
Subníveis p: orientados nos eixos cartesianos.
- l = 2: Subnível d (cinco orientações).

 Subníveis d: cinco orientações possíveis.
Subníveis d: cinco orientações possíveis.
Número quântico de spin (ms)
Indica a orientação do elétron ao redor do seu próprio eixo. Assume apenas os valores -1/2 e +1/2.
Resumo dos Números Quânticos
| Nome | Símbolo | Significado | Valores |
|---|---|---|---|
| Principal | n | Camada | 1, 2, 3... |
| Azimutal | l | Subnível | 0 a n-1 |
| Magnético | ml | Orientação | -l a +l |
| Spin | ms | Spin | 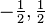 |
Origem dos números quânticos
Na teoria de Bohr, eram postulados. Na mecânica quântica moderna, surgem naturalmente da solução matemática da equação de Schrödinger.
Referências
- Atkins, P.; Jones, L. "Chemistry: molecules, matter and change".
- Mahan, B. M.; Myers, R. J. "Química: um curso universitário".
- Santos Filho, P. F. "Estrutura atômica & ligação química".
- Peruzzo, T. M.; Canto, E. L. "Química: na abordagem do cotidiano".
