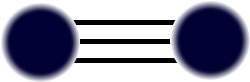Substância Pura: Tipos, Propriedades e Separação
Classificado em Química
Escrito em em  português com um tamanho de 60,44 KB
português com um tamanho de 60,44 KB
Substância Pura
As substâncias puras são aquelas formadas por apenas uma variedade de molécula. Ou seja, todas as moléculas são iguais. Por conta disso, possuem ponto de fusão, solidificação, ponto de ebulição constantes, e sua composição é bem definida.
Substância pura simples
As substâncias puras simples são formadas por apenas um elemento químico. Por exemplo, o gás Nitrogênio é composto apenas por átomos N:
Outros exemplos: H2, O2, O3 (ozônio), Fe, Al
Substância pura composta
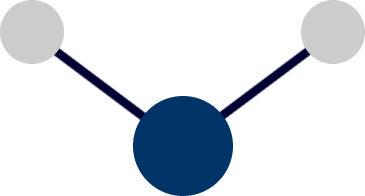
Já as substâncias puras compostas podem ter vários elementos químicos diferentes na mesma molécula.
Por exemplo, a água pura contém apenas moléculas H2O, mas, como sabemos, é formada pelos elementos químicos Hidrogênio e Oxigênio:
Outros exemplos: CO, NaCl, H2SO4, H2S
Sistemas: homogêneo e heterogêneo
Essas substâncias podem originar sistemas homogêneos e heterogêneos:
Sistema homogêneo
Apresenta apenas uma fase, que pode ser visualmente identificada. Exemplo: copo de água líquida. (1 fase; 1 ou mais componentes).
Sistema heterogêneo
Pode apresentar mais de uma fase, como um copo de água com gelo (tudo que está no copo ainda é água, apenas em estados físicos diferentes). (2 ou mais fases; 2 ou mais componentes).
Como calcular densidade
Massa = 1 kg
Volume = 2 litros
D = m / v = 1 / 2 = 0,5 kg/L
Processos de separação e mudança de estado
Solidificação
Líquido para sólido.
Liquefação
Gasoso para líquido.
Fusão
Sólido para líquido (aquecimento).
Condensação
Gasoso para líquido (resfriamento).
Evaporação
Líquido para gasoso.
Destilação
Separação de líquidos por diferença de ponto de ebulição.
Filtração
Separar sólido de líquido através de um filtro.
Decantação
Separação entre uma fase sólida e uma fase líquida ou entre duas fases líquidas.
Peneiração
Separar areia fina da areia grossa.
Separação por métodos manuais e físicos:
Catação: O processo de separação manual dos diferentes componentes (ou fases) que compõem uma mistura chama-se catação. Ex.: separar feijão dos grãos podres.
Levigação: Processo de separar os elementos mais densos dos menos densos utilizando água corrente; é a levigação.
Flotação: Para separar uma mistura de areia e pó de serra, por exemplo, basta colocar a mistura numa vasilha e juntar água. A parte menos densa da mistura (o pó de serra) flutua, enquanto a parte mais densa (a areia) fica no fundo da vasilha.
Ventilação: É o método de separação de substâncias sólidas de densidades muito diferentes, por meio de uma corrente de ar.
Separando misturas heterogêneas entre sólidos e líquidos
Filtração: Efetua o processo de filtração através de um filtro, que retém a parte sólida e deixa passar a parte líquida.
Decantação: Quando a parte sólida se deposita no fundo do recipiente, podemos despejar a parte líquida.
Centrifugação: Girando em alta velocidade, as roupas são lançadas contra a parede do tambor, enquanto boa parte da água é extraída das roupas.
Destilação: É o processo pelo qual podemos separar um líquido misturado a outro líquido ou a um sólido. A destilação é feita num aparelho chamado destilador.
Densidade
Quando se diz que um corpo tem uma densidade de 5, quer dizer que tem uma massa volúmica 5 vezes superior à da água (no caso dos sólidos e líquidos).
Imiscível: Não se mistura.
Miscível: Se mistura.
Polar: Moléculas com polos positivos e negativos.
Apolar: Não apresenta polos; moléculas não polares.